低溫冷等離子體清潔還原金屬氧化物
文章出處:等離子清洗機廠家 | 深圳納恩科技有限公司| 發表時間:2022-12-19
物質的狀態以固態��、液態����、氣態及等離子態(等離子體)存在����,宇宙中絕大多數的物質都是以等離子體的方式而存在�。固態物質中的粒子距離小���,當給固體物質提供能量如加熱的方式���,固態物質中的粒子間距會變大�����,從而轉變成液態物質����。若繼續提供能量時����,液態物質中的粒子間距繼續增大���,即會轉變成氣態物質��。宏觀物質的三種狀態的轉化已被人們廣泛熟知��。當繼續給氣態物質提供能量如提供電能或熱能時���,氣態物質的中的分子會被離解��,產生原子或其他單個分子�����;原子也會被電離形成離子��,核外電子脫離原子核的束縛變成游離電子�,由帶正���、負電荷的粒子組成的一種物質狀態即稱為等離子體��。等離子體是由帶電荷粒子組成的宏觀不顯電性物質�,等離子體的運動受到磁場的影響��。
當前的低溫冷等離子體還原技術主要應用的半導體制備����、微電子���、納米顆粒合成等諸多方面��。該等離子體具有處理溫度低�����,活性物質濃度高與反應能力強等特性�,能夠在常溫下清潔材料表面���,還原金屬表面氧化物���。
等離子體還原金屬氧化物原理:
低溫冷等離子體還原原理為:低溫下等離子體中的活性物質與材料表面的氧化物發生反應��,反應的活性物質為不同狀態的H粒子����,如原子態(H)��、離子態(H+,H2+,H3+)和激發態的H原子或分子(H*或H2*)等粒子等����。反應生成的易揮發的水蒸氣由等離子體本身的氣流將反應產物帶走�����,從而實現金屬表面氧化物還原的效果����。
然而H2在存儲����、運輸和使用方面均存在較大的安全風險����,但NH3作為一種相對存儲安全����,使用環境要求更低的氣體���,且NH3在高壓電場下被電離后也會形成多種具有還原性的物質足以能夠還原氧化物�����。NH3在高壓電場中被電離后形成的等離子體含有大量的還原性物質��,而且還原性物質的濃度隨著NH3比率增加而增加�����。
NH3-N2混合氣體等離子體還原Fe2O3反應
NH3-N2混合氣為工作氣體的常溫等離子體還原Fe2O3時���,NH3和N2混合氣體在高壓電場下分別被電離����、激發和離解����,反應產物之間會發生分解復合化學等反應��,整個形成等離子體階段為一系列的復雜電化學反應過程����。NH3-N2混合氣在高壓電場下被電離時����,N2在高壓電場下會按照反應式(1.1)~(1.3)等發生改變����,產生的電子e與激發態的氮分子N2*會參與到NH3的電化學反應過程當中NH3在高壓電場下發生離解��、電離和激發等反應�����。發生如下(1.4)~(1.10)等反應:
N2→N+N (1.1)
N2→N*+N*+2e (1.2)
N2+e→N*2+e (1.3)
NH3+e→NH2(或NH)+H(或H2)+e (1.4)
NH3 +N*2→NH2(或NH)+ H(H2) + N2 (1.5)
NH2+NH2+N*2→N2H*4+N2 (1.6)
NH+NH→N2H*2→N2+H2 (1.7)
NH+NH3→N2H4 (1.8)
H2+N*2→H*2+N2 (1.9)
H2+e→H+H (1.10)
不同的還原性粒子與固體氧化物Fe2O3的還原反應不一樣����,表1-1為不同還原性粒子還原Fe2O3的反應式�����。表中式(1.11)為聯氨還原Fe2O3的化學反應式�����,等離子體中活性粒子能量較高�����,比常規的化學反應應更容易進行���。表中式(1.12)與(1.13)為原子態H還原Fe2O3的變化過程����,原子H一直被認為是氫等離子體中最重要的還原性粒子�����。表中式(1.14)為激發態分子氫H2*還原Fe2O3的變化過程��。等離子體中具有多種還原性物質��,諸多物質對還原反應過程相互影響�。常溫等離子體還原Fe2O3的反應過程表現為過渡還原����,即Fe2O3先被這些還原性物質還原成Fe3O4���,再還原成金屬Fe���。
表1-1不同還原性粒子還原 Fe2O3 反應式
上標“*”為該物質處于激發態
圖1為常溫等離子體還原Fe2O3過程的示意圖��,不同比率的NH3-N2混合氣在高壓電場下形成等離子體后產生多種還原性的物質�,如N2H4�、H和H2*等���。等離子體先將高價氧化物Fe2O3還原成低價態鐵的氧化物Fe3O4��,接著被還原成金屬Fe�����。隨著還原反應的進行���,固體氧化物Fe2O3中的O原子不斷被剝離出試樣表面使得Fe2O3表面體積收縮���,形成局部坍塌現象����,微觀上呈現出孔隙變大���、裂縫變寬等形貌特征�����?��?紫兜男纬膳c擴大為還原性活性物質進入固體氧化物Fe2O3的內部提供了有利條件�����。而還原反應進行到一定階段時����,固體氧化物Fe2O3表面形成一層致密的金屬Fe后���,包覆在Fe2O3表面的金屬Fe會限制等離子中活性物質在反應界面的擴散從而影響還原反應的進行�����。
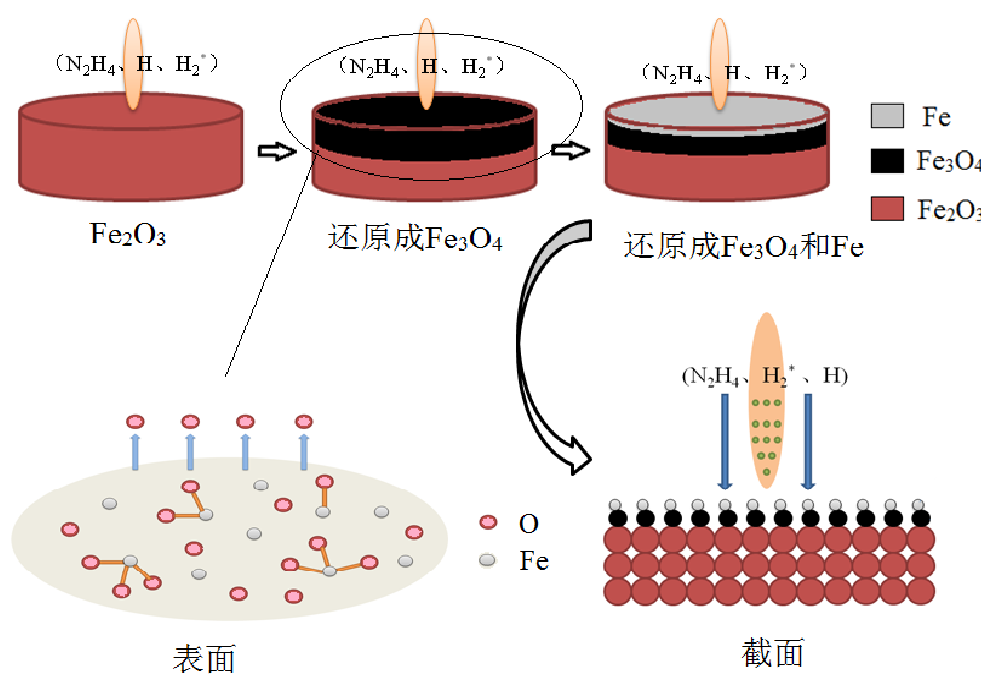
圖1 等離子體還原過程示意圖
等離子體中的高能活性粒子在碰撞�、濺射過程中把能量轉移到金屬氧化物粒子上�,使表面部分區域的能量升高出現一些反應活性點��,還原反應首先在這些能量高于活化能的活性點上發生�����,并且活性點的數量逐漸增多���,促使還原反應向橫向和縱向推進�,但是還原過程中伴隨著產物的氧化整個還原過程是一個還原反應和氧化反應相互競爭最后達到動態平衡的過程�����。

